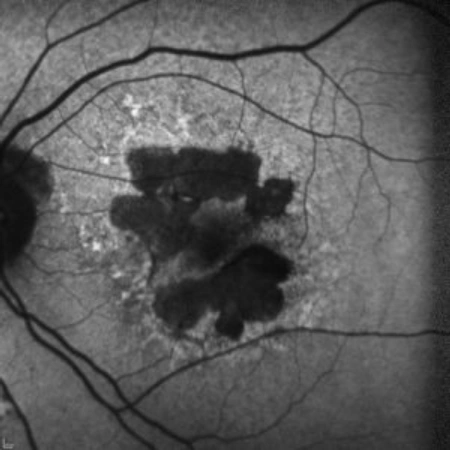
La degeneració macular associada a l’edat (DMAE atròfica), també coneguda com a degeneració progressiva de la màcula, és la primera causa de pèrdua de visió en pacients de més de cinquanta anys en el món occidental. Amb més de 25 milions de persones afectades arreu del món, es calcula que cada any uns 500.000 nous casos es registren. Aquesta malaltia té una base genètica, però els factors epigenètics, com els hàbits de vida i els factors ambientals, juguen un paper fonamental en la seva progressió. De fet, la microbiota intestinal ha demostrat influir-hi de manera important. L’Institut de la Màcula és pioner en la recerca de l’impacte de la microbiota a la progressió de les diferents formes de la DMAE.
Subclasses de DMAE i estadis de la malaltia
La DMAE es divideix en tres estadis:
- DMAE primerenca: S’observen dipòsits petits de brossa en les capes externes de la retina, pel mal funcionament de les cèl·lules retinals, especialment l’epiteli pigmentari.
- DMAE intermèdia: Els dipòsits augmenten de mida, els canvis degeneratius es fan més visibles, i comença a afectar la funció visual.
- DMAE avançada: En aquest estadi, les cèl·lules retinals moren, provocant la pèrdua irreversible de la visió central. Aquesta fase inclou la DMAE atròfica (morta de les cèl·lules de la retina), que pot evolucionar ràpidament.
La DMAE atròfica és una de les formes més greus i pot causar la pèrdua de visió en pocs anys. A mesura que la malaltia avança, les zones de mort retinal creixen, i això acaba afectant la visió de manera irreversible.
DMAE “seca” vs. DMAE atròfica
Sovint, es parla de la DMAE seca, però és un terme confús. Alguns el fan servir per referir-se a la DMAE intermèdia, mentre que altres l’associen directament a la DMAE atròfica. La DMAE intermèdia implica l’acumulació de dipòsits de brossa degut a l’alteració de les cèl·lules de l’epiteli pigmentari. Amb el temps, aquestes cèl·lules moren i provoquen l’inici de la DMAE avançada en la forma atròfica, que implica la mort progressiva de la retina i la pèrdua de visió irreversible.
Teràpies per a la DMAE atròfica
El Prof. Jordi Monés ha estat un pioner en el desenvolupament de teràpies emergents per a la DMAE atròfica. El 2005, va impulsar la recerca amb l’empresa biotecnològica Ophtohotech per utilitzar tractaments anti-VEGF en pacients amb DMAE atròfica. Aquestes investigacions van portar al desenvolupament d’un tractament anomenat Avacincaptad Pegol, que ha mostrat resultats significatius en la prevenció de la progressió de l’atròfia geogràfica. Això representa un avanç important per al tractament d’aquesta malaltia.
Actualment, també s’estan investigant tractaments amb teràpia gènica, com els assaigs clínics en fase 3 a l’Institut de la Màcula i altres tractaments dissenyats pel Dr. Monés en el camp de la teràpia gènica als Estats Units.
Prevenció de la DMAE
Tot i que no existeix un tractament per prevenir la malaltia directament, millorar l’estil de vida pot ajudar a no agreujar-la. Les següents recomanacions són fonamentals:
- No fumar.
- Mantenir una dieta sana: rica en fruites i verdures i baixa en greixos d’origen animal.
- Fer exercici de manera regular.
- Mantenir un pes saludable.
- Adoptar hàbits saludables de son, dormint almenys 7 hores al dia.
La DMAE atròfica és una malaltia complexa que afecta milions de persones a nivell mundial, però els avenços en la recerca i les teràpies emergents ofereixen esperança per als pacients afectats.