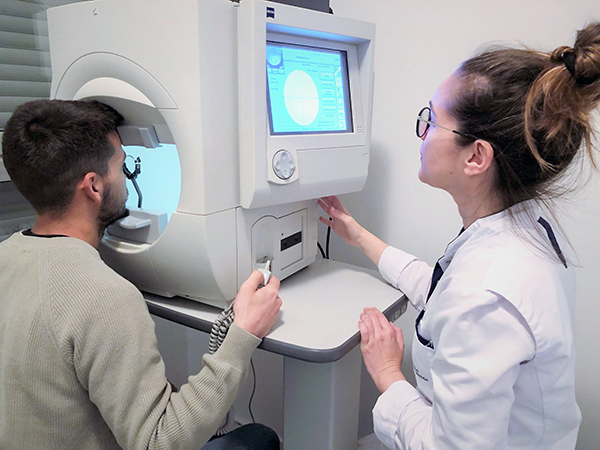
La campimetria visual és un examen que s’empra per a valorar les alteracions del camp visual (porció d’espai que és capaç de captar l’ull mentre està enfocat en un punt central).
Gràcies a aquest examen es detecta qualsevol mena de pèrdua de la visió perifèrica i s’obté, a més, un mapa d’aquesta pèrdua que orienta i ajuda a l’hora de fer el diagnòstic de certes patologies (glaucoma, malalties de la retina, lesions de la via òptica, etc.).
En aquesta mena d’examen el pacient roman assegut davant del campímetre (aparell amb la part interior de forma esfèrica). S’examinen els dos ulls de manera independent, de manera que cal mantenir tancat un dels ulls del pacient mentre l’examinador li demana que vagi indicant quan veu un feix lluminós intermitent i de diferents intensitats. Aquest flaix lluminós va apareixent en zones diferents del camp visual de l’ull estudiat. Posteriorment, es repeteix la mateixa exploració per a l’altre ull.
Per a aquesta mena d’estudi, que és totalment indolor i no presenta contraindicacions, no es requereix cap preparació prèvia per part del pacient.